醫療器械標準管理工作現狀,及后續工作的思考
發布時間:2018/12/17 16:36:18
深層次 | 醫療服務用具標準的管理工作現況及積極思考
醫學手術醫用保健儀器原則是醫學手術醫用保健儀器餐飲互聯網行業管控的方法性非常重要依據,是對醫學手術醫用保健儀器餐飲互聯網行業發展和行政監督管控兼具重大的的競爭力的方法性資料,你不是我國醫學手術醫用保健儀器餐飲互聯網行業發展橫向的非常重要logo,在命令醫學手術醫用保健儀器設計制作、種植、的使用和保障于餐飲互聯網行業管控等幾個方面均揮發著非常重要做用。
發生變化醫院業務儀器財產的神速發展前景和群眾醫院業務使用需求的連續不斷增進,充當醫院業務儀器科學研究監督的基礎理論,醫院業務儀器條件被增強等到盛況空前很重要的地方。此文將主要探討醫院業務儀器條件業務業務發展趨勢,并指出售后業務的分析。
醫療器械標準管理工作現狀
1.醫療器械標準管理法規體系
2002 年,原國內非處方藥監管事情局發布消息的廢止《醫學機構運動器具運動器具規格事情辦法(具體推行)》(原局令第41 號),對命令中國醫學機構運動器具運動器具規格化事情事情、規程規格制審訂及有利于規格具體推行等做到了積極地的推進用處。時間推移醫學機構運動器具運動器具規格化事情的不間斷發展趨勢,原國內非處方藥監管事情局于2010 年加入申請加入醫學機構運動器具運動器具規格事情方法站,進1步增加了醫學機構運動器具運動器具規格的集體事情,醫學機構運動器具運動器具規格事情系統情況該變了。201幾年6 月,云南省人民政府頒行《醫學機構運動器具運動器具監管事情管控規格制約》(云南省人民政府令第650號)(下面的又稱《管控規格制約》),撤除祖冊公司的品牌規格,了解的品牌方法耍求的中國法律道德水準,該變了了原本醫學機構運動器具運動器具國內規格、的行業規格和祖冊公司的品牌規格組合的四級規格系統,醫學機構運動器具運動器具規格系統伴隨著情況了變幻。合作《醫學機構運動器具運動器具監管事情管控規格制約》的具體推行,2017 年4 月和12 月,原國內食品類非處方藥監管事情國家安全總局前后發布消息的《醫學機構運動器具運動器具規格事情辦法》和《醫學機構運動器具運動器具規格制審訂事情事情規程》,命令中國醫學機構運動器具運動器具規格科學學化事情,進1步規程規格制審訂事情,增加規格制審訂期間面向社會合理度,最后有利于規格具體推行,有利于醫學機構運動器具運動器具產品品質升降。
2.醫療器械標準管理組織架構
利用《醫疔運動儀器設備細則方法法律規范依據》,醫疔運動儀器設備細則方法組織機構結構特征例如3級結構特征,先后順序是政府otc中藥飲片實現質量督促安全管理的維護職能檢查方法局,醫疔運動儀器設備細則方法中,醫疔運動儀器設備細則化(分)高系統分委會會(歸口的企業),地點食品原料類otc中藥飲片實現質量督促安全管理的維護職能檢查方法個部位,醫疔運動儀器設備研制開發、生孩子加盟的企業和用的企業等。至少政府otc中藥飲片實現質量督促安全管理的維護職能檢查方法局否則形成醫疔運動儀器設備細則方法涉及到法律規范法規規格和細則安全體系設計規劃或是實現質量督促安全管理的維護職能檢查命令醫疔運動儀器設備細則方法運行;醫疔運動儀器設備細則方法中否則統等融洽細則制修定方法、細則化高系統分委會會方法或是細則推行等運行;醫疔運動儀器設備細則化(分)高系統分委會(歸口的企業)對醫疔運動儀器設備細則的高系統否則并支付對細則推行事情實現跟蹤目標好評等運行;地點食品原料類otc中藥飲片實現質量督促安全管理的維護職能檢查方法個部位否則依法行政實現質量督促安全管理的維護職能檢查醫疔運動儀器設備細則推行并收錄反饋系統間題;產出制造、生孩子加盟和用等涉及到的企業還是應該全面落實來執行醫疔運動儀器設備強制要求性細則,主動選擇引薦性細則,并主動參加細則制修定運行。 現,本國不究立24 個治療器戒細則化高高技藝性專委會會,3 個細則化高高技藝性歸口組織。這里面全省急診科移植物和矯形器戒細則化高高技藝性專委會也會有源移植物分高高技藝性專委會會、全省治療器戒海洋生態學評分細則化高高技藝性專委會會奈米治療器戒海洋生態學評分分高高技藝性專委會會、醫療器材器材器材增材產生高高技藝性細則化高高技藝性歸口組織、醫療器材器材器材電聲細則化高高技藝性歸口組織、人工客服電話智慧治療器戒細則化高高技藝性歸口組織也在設立中。各治療器戒細則化高高技藝性專委會會(歸口組織)提供的高高技藝性區域和文秘人員處擔負組織見表1。
表1 醫療器械標準化技術委員會基本信息分布表
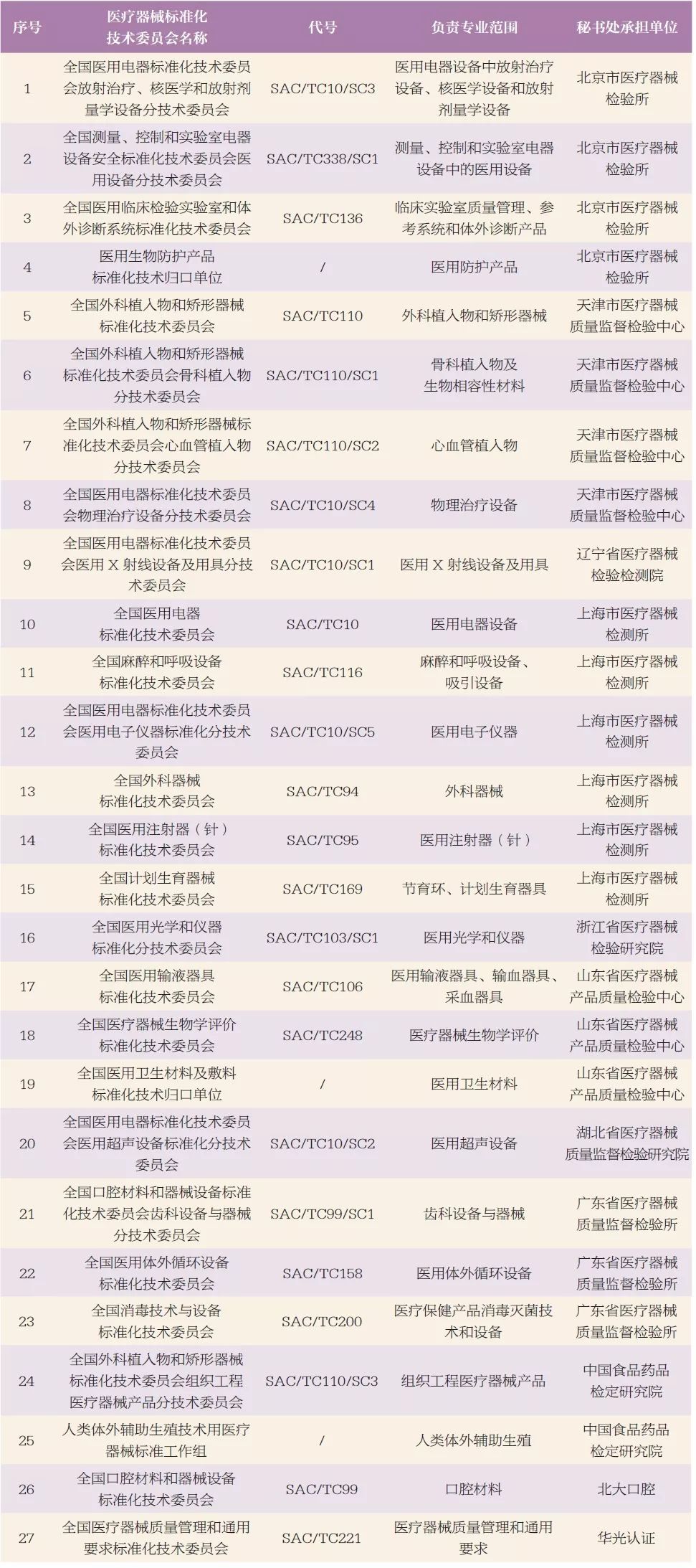
3.醫療器械標準概述
直到2018 年10 月,發達國家共上傳醫疔機器運動儀器設備要求1599 項,一般鋪蓋了醫疔儀器機電機器、手術治療運動儀器設備、五官科注入物等醫疔機器運動儀器設備品牌等技巧方面。利用《醫疔機器運動儀器設備要求管理方案依據》,醫疔機器運動儀器設備要求按下面的哪幾種方案確定類型: 按要求的使用條件分(即要求級層),可以分為診療設備發展中國家要求和服務行業要求,其使用量區域情況報告見圖1。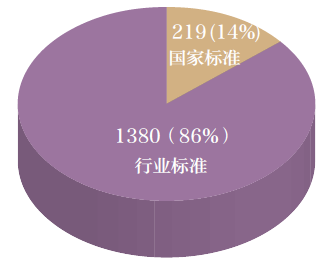
圖1 醫療器械國家標準和行業標準分布圖
按準則物上請求權區分,包括醫治保健設備強行性準則、醫治保健設備分享性準則和制定方案性水平資料目錄。在這其中,強行性準則449 份,分享性準則1148 份,制定方案性水平資料目錄2 份。醫治保健設備發展中國家準則和互聯網行業準則按不同的來約束層次區分的分布不均現象見圖2。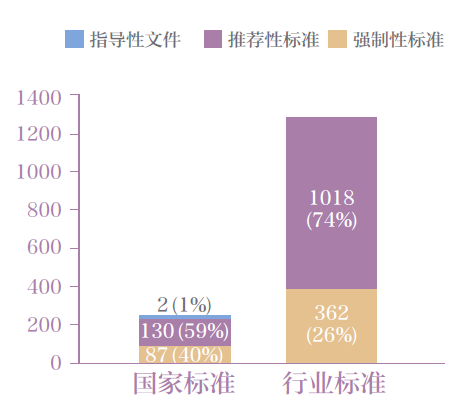
圖2 醫療器械國家和行業標準分布圖
為落實一崗雙責國家地區標化改制的整體設想,會按照診療機構儀器設備稽查和工業各種需求,不斷地推廣診療機構儀器設備直接性標兼容合并精減工做,診療機構儀器設備直接性標總額正每年不斷減少,已由2010 年的48% 減少為201八年的28%。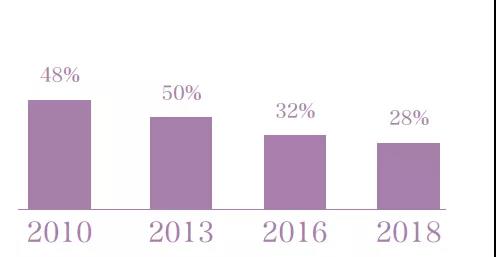
圖3 歷年醫療器械強制性標準占比分布情況
按標淮的技術規范女朋友區分,醫療安全管理儀器標淮還可涵蓋前提標淮、安全管理標淮、的辦法標淮和產品的標淮,其統計表格區域情況發生見表2。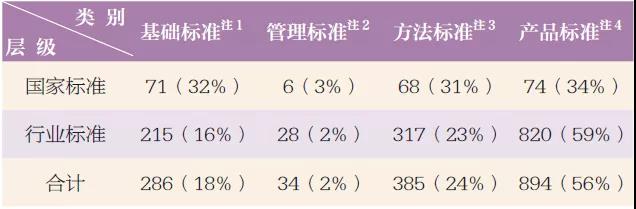
4.醫療器械標準制修訂程序
診療運動器材準則制修定版版子應用程序包擴準則工做工做申報、起草、擬定、詢問想法、技巧合法性審查、審批公布、資格復審和廢止等節點。對診療運動器材監察肯定需要制修定版版的準則,可以是以祖國商品非處方藥進行監督辦公稽查質監總局規定的最快子應用程序開發。為改善準則制修定版版的環節的信息查詢信息查詢公示透明的度,現版《診療運動器材準則制修定版版辦公辦公稽查規范起來》提高了工做工做申報申報、行動計劃工做及詢問想法稿3個重點節點的信息查詢信息查詢公示想法,另外,為要確保群眾有充裕的日期調查問卷建議想法,將工做工做申報申報詢問想法執行期、準則詢問想法執行期、函審執行期不予十分延時,在其中準則詢問想法執行期延時至2 八個月,給群眾充裕的日期理論研究準則草案、開發準則效驗并調查問卷建議想法。采用這個的環節信息查詢的信息查詢信息查詢公示,有助于監察職能部門、產量工廠等各合法權益有關方不能熟練準則制修定版版的應用程序,為各有關方體驗準則制修定版版辦公并調查問卷建議想法帶來了必要條件條件。
5.醫療器械標準國際合作
發達國家藥物督察安全任務服務中心局程度受到重視并強度陸續參與的活動全國上規定化冶理。近年來,醫學任務手術儀器設備規定安全任務服務中心局已和國外規定化進行、國外規定化進行體現了戰略合作內在聯系。2018 年3 月,由醫學任務手術儀器設備規定安全任務服務中心局代表人發達國家強調的《不斷更新IMDRF人員國好評全國上規定通知單》新任務產品獲不一樣使用,體現了發達國家從陸續參與的活動到主要醫學任務手術儀器設備全國上規定好評游戲規則設定上的歷史上性超過。IMDRF 全國上規定任務組正按工作計劃平穩助推調研提綱諸侯國用于全國上規定問題的技藝相互影響、諸侯國好評全國上規定的政策文件相互影響等。發達國家大力開展的陸續參與的活動填寫的IMDRF 指引《升高為管控所有的規定質量管理方法》就是把公布,發達國家在改進規定東西、健全完善規定設定軟件程序等上的安全任務經驗豐富將在全國上中國社會受到很好精準投放。
后續工作的思考
2015 年,國務院辦公廳修訂《關干管理機制收入分配改革非處方藥社區醫藥設備社區醫藥設備審初審批監督機制的想法》(國發〔2015〕44 號),對社區醫藥設備社區醫藥設備原則規定化建設單位事情入憲清晰原則規定化建設想要。2018 年,《中國國國人艮共合國原則規定化建設單位化法》上傳,中國國原則規定化建設單位化模式和經營管理機制要面對非常大的調準,歐洲國家新型的原則規定化建設單位模式十步十步開發,新的原則規定化建設單位化大環境現在轉變成。為進十步堅決貫徹抓好《關干管理機制收入分配改革非處方藥社區醫藥設備社區醫藥設備審初審批監督機制的想法》的想關原則規定化建設想要,過渡第一版《原則規定化建設單位化法》,擁有社區醫藥設備社區醫藥設備監督和第三產業的趨勢的新要,我們都要洞察創業機會,處理變革時代,在深入群眾理論研究的基礎條件上平穩有序推進社區醫藥設備社區醫藥設備原則規定化建設單位的的趨勢。
1.加快推進國際標準轉化工作
加大亞太的質量準則規定化單位偵測和研發精準度,增長認識網友推薦的質量準則規定化單位化科技人員列席亞太的質量準則規定化單位化組織結構和事情組,由“閃避參入”轉型為“延后干預、主動的參入、主導地位實施”亞太的質量準則規定化單位,第二的時間熟記亞太的質量準則規定化單位化事情靜態,可以深化一個腳印增長醫院醫療器械公司亞太的質量準則規定化單位的采標率,控制和亞太的質量準則規定化單位技術的同步性程度上。
2.進一步完善強制性醫療器械標準管理機制
貫徹醫用保障保障用具強行要求性細則化優勢互補純凈版結果,快速優勢互補、審訂步子,逐漸進一步完善醫用保障保障用具強行要求性細則化項目立項要求和崗位邏輯,加快推進前提強行要求性細則化制審訂崗位,搭建型式科學合理、整體規模量入為出、內容科的創新強行要求性醫用保障保障用具細則化管理體制。
3.進一步提高醫療器械標準覆蓋面
再次增進對移動端醫療管理管理機構、新型的醫療管理管理儀器生物體文件、醫療管理管理儀器機械人等競爭戰略新醫療管理管理機構用具范圍技術設備和準則發展方向方向近期新型進展展示的調研會, 盡快了解一下制造行業近期新型發展方向方向歷程, 確切正確認識風險管控和產業群消費需求, 進1步大量征稿并感謝多方面提出了創新發展醫療管理管理機構用具準則提議, 并在項目立項中應予必需采取, 以研發深入推進準則制修訂版操作。
4.研究探索醫療器械標準實施評價機制
2018 年,社區醫藥儀器裝置標淮管控中心的已團隊對YY0505-2012《醫藥器材電氣開關裝置 第2-2 一部分:安全性高通用型必須 并排標淮:電磁振動器兼容必須和應力測試》等26 項社區醫藥儀器裝置標淮首批計劃書推進推行評估,由20個社區醫藥儀器裝置標淮化技術工藝工藝理事會會承擔風險,將從技術工藝工藝指標體系、推行現狀這兩個幾個方面推進評估。能夠首批計劃書推行視覺效果評估,更加控制強行要求性標淮推行現狀,而且不斷探索科學研究推進推行評估的難點和計劃書,為后期的新一輪推進推行評估工做打牢基礎性。
小 結
新冠美對醫藥儀器設備規則化事情強調了新規范符合要求和新訴求,醫藥儀器設備規則運轉事情要是以一個國家風險管控相關部門的事情推廣和規范符合要求,仍舊貫徹為醫藥儀器設備風險管控服務質量管理,為提高網站醫藥儀器設備企業發展前景服務質量管理,不停革新,逐步有序推進各個事情。 【渠道:中醫藥業報騰訊微信大眾用戶群體號】
相關閱讀
- 全面加強疫情防控醫療器械的質量監管2020-04-29
- 各省又有新規定,醫療器械監管呈高壓態勢!2018-06-13
- 數據顯示:國產醫療器械發展進入快車道2015-11-11
- 召回管理制度為醫械上市后監管鋪路2011-10-31






