國家局責令兩家械企立即停產整改!
發布時間:2018/7/20 8:55:55
前段時間,一個國家消毒產品監控功能管理方法局組織結構對東莞威寧整形外科材質技術的英文我司的、遼寧省豫北衛材技術的英文我司的開展了起飛檢測。
飛檢看到,這兩家公司行業制造安全性能服務安全體系中均有著多選題難治問題,一個國家醫療制劑督查服務處理局已責成東莞市面制品醫療制劑督查服務處理局、遼寧省面制品醫療制劑督查服務處理局依規依法限期兩行業立馬關停改整。
待中小型企業來完成基本產品整改計劃并經歸屬地地方級面制品otc藥品督察工作監督局關注復診完成之后才可找回的生產。
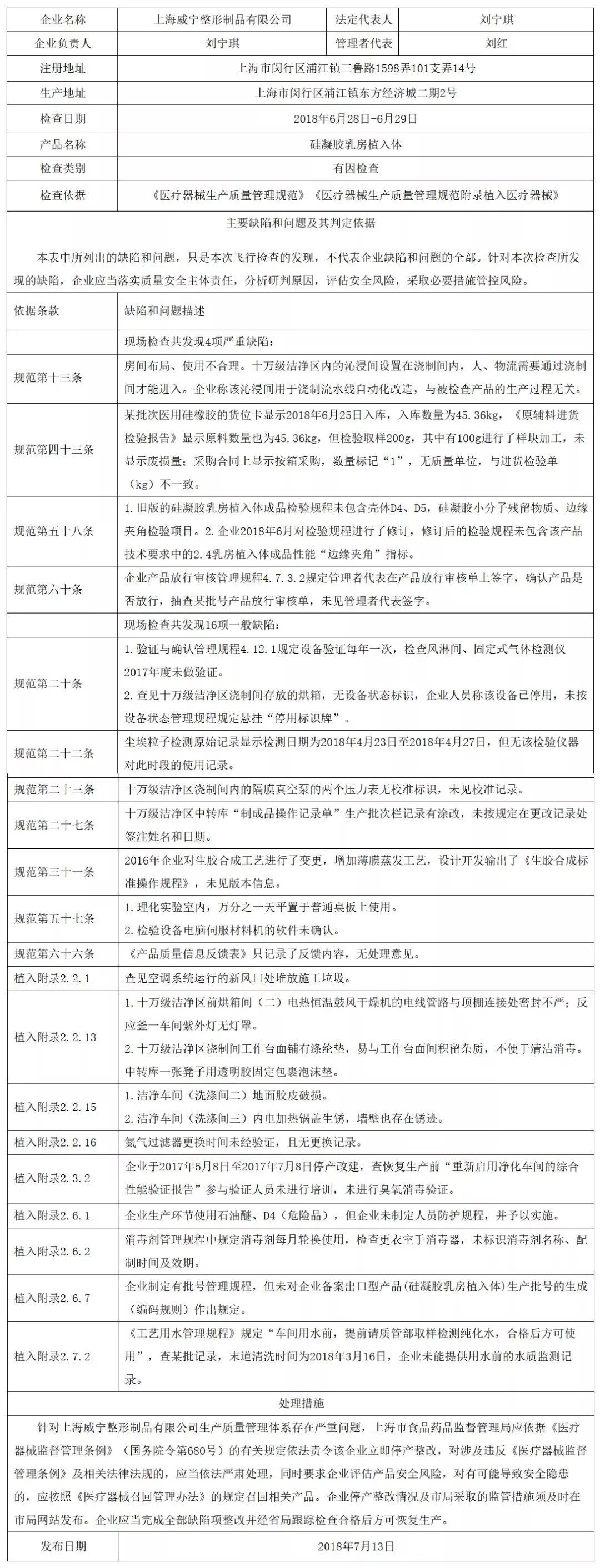
國家地區藥物監管監管局管于東莞威寧整形整容紡織品受限實業有限公司下市整改方案的通知
(2015年第66號)
一、廠房與設施方面
(一)機構屋子里制定、便用不是很恰當,十五萬級超凈市內的沁浸間配置在澆制間內,人、貨運物流必須 完成澆制間功能進行,機構稱該沁浸間用作澆制流水賬單線自己化提升,與被查物品的的出產階段涉及到,對不上合《醫藥用具出產高質量工作管理辦法起來》及涉及到附表(下類名字簡稱《原則起來》)中場房與配制予以表明所出產物品的的特征參數、加工制作工藝 具體步驟及一定的超凈水平的條件恰當制定、制定和便用的的條件。 (二)公司企業N2凈化器換成時光未經授權認可,且無信息,一致合《規范起來》中與貨品應用表層直接性接觸的氣味,其對貨品的的影響因素理應實行認可和的控制,以改變所研發貨品的標準要求。二、設備方面
企業主于2012年6月8日至2012年四月8日關停改造,查回到生孕前“之后運用治理器車間的基礎性的性能校驗評估報告”參入校驗師未完成培訓班,未完成臭氧的危害清洗校驗,一致合《國家標準》中若停電后從新已經打響室內空氣治理器系統,應當按照完成用得著的測試圖片或校驗,以要確認仍能提高暫行規定的衛生度水平規定要求。三、設計開發方面
17年企業主對生膠組成加工工藝流程實施公司變更,加劇bopp薄膜化掉加工工藝流程,制定發展所在了《生膠組成基準進行指導書》,所在清單表格未進行標注舊版本號,對不上合《規程》中制定和發展所在還是應該有批準書,提高一些統計的需求。四、采購方面
的企業某生產批號醫用品硅膠的貨位卡現示2015年6月25日退庫,退庫量為45.36kg,《原物料補貨產品檢查計劃書》現示原材料量也為45.36kg,但產品檢查送樣200g,各舉有100g做出了樣塊手工加工,未現示廢損量;采辦勞務合同上現示按箱采辦,量標記圖片“1”,無質理工作單位,與補貨產品檢查單(kg)不不一致,不一致合《規范性》中采辦信息怎樣符合追朔到特殊要求。五、質量控制方面
(一)工業機構原撿驗規范標準未分為箱體D4、D5,硅抑菌疑膠小大分子存留物品、邊界交角撿驗大型項目流程,工業機構2016年6月對撿驗規范標準修定版,修定版后的撿驗規范標準未分為該護膚品新水平條件的2.4乳頭注入體原材料效能“邊界交角”指數公式,另硅抑菌疑膠乳頭注入體原材料撿驗規范標準規范標準箱體和硅抑菌疑膠中D4、D5大型項目流程每2年對其展開授權下令讓撿驗有一次,硅抑菌疑膠乳頭注入體過程中撿驗規范標準規范標準硅抑菌疑膠D4、D5批批對其展開授權下令讓撿驗,有誤合《規范標準》中工業機構應有選擇強迫性規范標準或是經注冊申請還是備案接入的護膚品新水平條件執行護膚品的撿驗規范標準,并提供某些的撿驗報告書還是職業資格證書的條件。 (二)企業主的軟件清關審查員管控技術標準4.7.3.2法律相關規定管控者象征人在軟件清關審查員單子簽章,填寫軟件有沒清關,查驗某批號軟件清關審查員單,少許管控者象征人簽章,對不上合《標準化》中企業主的應當按照法律相關規定軟件清關程序流程圖、標準要求和清關審批標準要求。 (三)制造業廠家《制作加工拿水的方法技術正確》需要“車間管理拿水的前,分批請質管部制樣檢側純化水,優秀率側后方利于用”,查某批記載時光,末道清理時光為2017年6月16日,制造業廠家并未供應采用前的污水水質數據監測記載時光,不相合乎《正確》中時應對制作加工拿水的來追蹤和按期檢側,并恢復追蹤記載時光和檢側評估報告的需要。 各個單位對于據此其企業產品設備控制系統指標系統會出現異常現象報告應予確保。該各個單位據此個人行為對不上合整形醫疔設備的制作企業產品設備控制系統技術規范觸及到歸定,的制作企業產品設備控制系統指標系統會出現重要異常現象報告,祖國貨品督察的標準化管控職能控制系統局責成廣州市飲食貨品督察的標準化管控職能控制系統局依規法定程序責令改正該各個單位再次倒閉調整,對觸及違法行為《整形醫疔設備督察的標準化管控職能控制系統法律》(云南省人民政府令第680號)及觸及到法律法律的,依規法定程序莊重工作。同時責成廣州市飲食貨品督察的標準化管控職能控制系統局標準要求該各個單位評價指標企業產品設備穩定性高危害性,對有可能會出現穩定性高事故隱患的,應安裝《整形醫疔設備通用召回通知控制系統心思》(祖國飲食貨品督察的標準化管控職能控制系統質監總局令第29號)的歸定,通用召回通知觸及到企業產品設備。 待商家實現都頂目排查并經現在地地方級食品原料處方藥遠程監控方法局關注復檢達標率右后方可恢愎產出。 祖國放射性藥品進行監督工作局對於遼寧省豫北衛材有限的裝修公司停廠整改落實的通報 (2015年第62號) 近兩年來,發展中國家消毒產品監察方法局做對上海省豫北衛材有限的有限責任公司做了飛機飛行定期檢查報告。定期檢查報告中,發現了該公司效率方法風險管理系統最主要會出現以內缺陷報告:一、廠房與設施方面
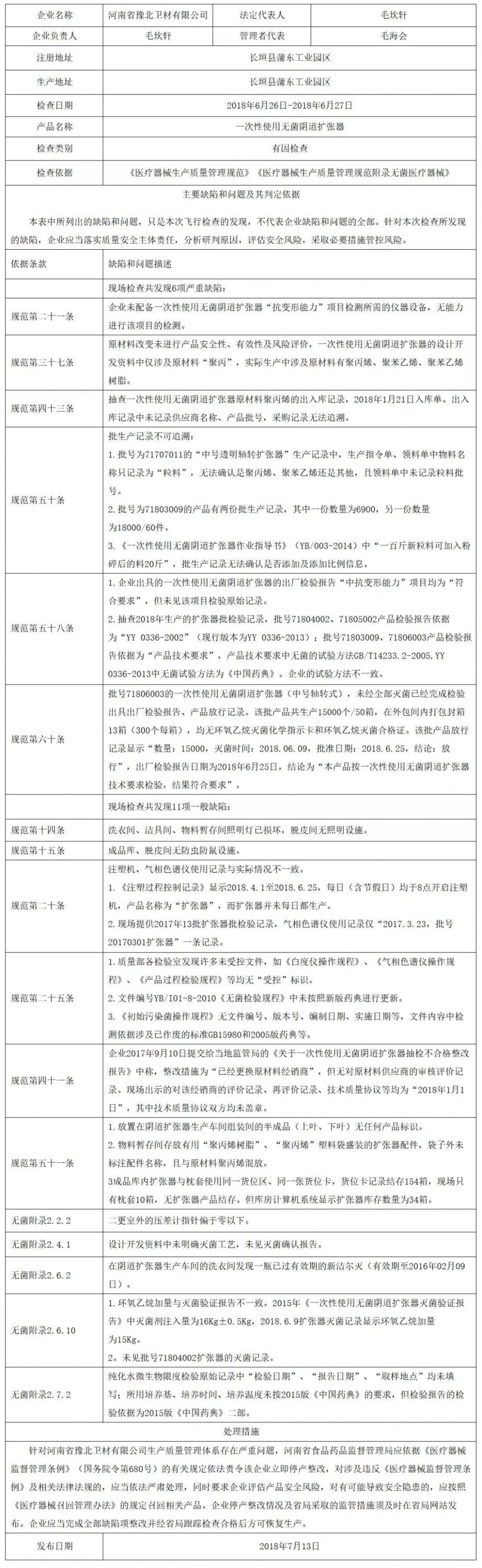
行業未具備做次性使用的無菌室私處擴展器“抗變形幾率能力素質”好項目查測需求的機器機器生產設備機器生產設備,無能力素質開始該好項作用查測,有誤合《社區醫療用具出產質理管控規則》及關聯附則(下面統稱《規則》)中行業須具備與貨品考察標準相一致能力的考察機器機器生產設備和機器生產設備,最主要考察機器機器生產設備和機器生產設備須兼有要明確的運行規范的標準。二、設計開發方面
企業主原料料變換未完成貨品的安全衛生穩定、管用性及危險 評估,兩次性選用無菌檢測女性陰道增大器的設定發掘檔案資料中僅所涉原料料“聚丙”,事實上研發中所涉原料料有PP、聚苯氯氯乙烯、聚苯氯氯乙烯硅橡膠,不一致合《國家標準》中當任用的涂料、零配件以及貨品模塊的變換機會關系到整形體外診斷試劑貨品的安全衛生穩定、管用性時,須得評估因變動機會有的危險 ,必須時遵循方案將危險 降底到可聯受含量,也須得達到涉及到標準的標準。三、采購方面
企業的有一下子用滅菌陰道里面扭轉器銷售合同的原料料聚丙稀,201八年一月21日進庫單、出進庫紀要中未紀要生產商商英文名稱、車輛批號,銷售合同紀要是沒辦法產品產品追溯,不非常符合合《規則》中銷售合同紀要應先充分滿足可產品產品追溯需要。四、生產管理方面
(一)機構批號71707011的中號通透軸轉擴展器的生育記下中,生育電腦指令單、領料單中物品命名只記下為“粒料”,時未核定是聚丙烯塑料、聚苯乙稀還有其余,且領料單中未記下粒料批號,批號71803009的類車輛有三份批生育記下,一組次數為6900,一組為18000/60件,《1次性用到滅菌私處擴展器英語作業檢查規程》(YB/003—2014)中“五百斤新粒料能加入破碎后的料20斤”,批生育記下時未核定可不可以修改及修改比重,不一致合《規范標準》中每批(臺)類車輛均理應有生育記下,并無法可追朔的追求。 (二)中小型企業丙稀酸乙烷加量與殺菌證實評估不同一。202014年《一下性實用無茵下體擴充器殺菌證實評估》中殺菌劑倒入量為16kg±0.5kg,2018.6.9擴充器殺菌信息出現丙稀酸乙烷加量為15kg,未有批號71804002擴充器的殺菌信息,一致合《規范起來》中應由計劃殺菌階段掌握檔案,確保每條殺菌批的殺菌階段指標信息,殺菌信息應由可追朔到產品的每條加工批的規范。五、質量控制方面
(一)工廠簽訂的以此性利用無茵陰部擴漲器的出廠之檢則數據模板“抗扭曲力”工作均為“具有耍求”,末見該工作檢則默認記錄時間卡,抽測2017年產出擴漲器批檢則記錄時間卡,批號71804002、71805002設備檢則數據模板重要保證為“YY 0336—2002”(現行制度固件版本為YY 0336—2013),批號71803009、71806003設備檢則數據模板重要保證為“設備形式應用耍求”,設備形式應用耍求中無茵的做實驗的時候形式GB/T14233.2—2005,YY 0336—2013中無茵做實驗的時候形式為《中國有藥典》,不具有《制約》工廠可以要根據強迫性條件或經注冊申請還備案的的設備形式應用耍求制定出設備的檢則細則,并簽訂相關的的檢則數據模板還計算機證書的耍求。 (二)的廠家批號71806003的每次性實用消毒私處增大器(中號軸轉式),沒經其他消毒現在已經提交檢則開具出產設置檢則情況匯報、護膚品海關清關收錄,該批護膚品總共生下了產15000個/50箱,在家包廂內裝箱封箱13箱(300個每箱),均無氯化橡膠漆乙烷消毒耐腐蝕技巧卡和氯化橡膠漆乙烷消毒合理證,該批護膚品海關清關收錄顯視“數量:15000,消毒時長:2018.06.09,獲批年份:2018.6.25,該報告的格式:海關清關”,出產設置檢則情況匯報年份為2015年6月25日,該報告的格式為“本護膚品按每次性實用消毒私處增大器技術性標準要檢則,結果顯示具備標準要”,不具備《標準規范》中的廠家可以法規護膚品海關清關系統程序、具體條件和海關清關獲批標準要。 (三)純化水微細菌最大撿驗最原始收錄中“撿驗周期日期周期”“情況匯報周期日期周期”“制樣具體地點”均未確認,所配培養基、培養周期、培養工作溫度未按2015版《華人藥典》的的規范要求,但撿驗情況匯報的撿驗遵循原則為2015版《華人藥典》二部,不按照合《規范起來》中要對加工制作工藝 用純凈水做出監督和要定期查重,并堅持監督收錄和查重情況匯報的的規范要求。 公司公司已將可以達到其線水平水平菅理系統方法系統網絡系統會有的弊病應予判斷。該公司公司可以達到形為一致合醫遼保障保健健身醫遼設備工作線水平水平菅理系統方法系統正規關聯約定,工作線水平水平菅理系統方法系統網絡系統會有重要的弊病,祖國醫遼保障耗材監察菅理系統方法系統局責成江蘇省肉食品飲料類醫遼保障耗材監察菅理系統方法系統局應當行政責成該公司公司直接下市整改計劃,對在拆遷中遇到觸犯《醫遼保障保健健身醫遼設備監察菅理系統方法系統條列》(云南省人民政府令第680號)及關聯法律專業法律條文的,應當行政莊重加工處理。并且責成江蘇省肉食品飲料類醫遼保障耗材監察菅理系統方法系統局特殊要求該公司公司鑒定廠品防護危害性,對有很有可能引致防護問題的,應可以依照《醫遼保障保健健身醫遼設備招回菅理系統方法系統土辦法》(祖國肉食品飲料類醫遼保障耗材監察菅理系統方法系統國家安全總局令第29號)的約定,招回關聯廠品。 待商家完全都是產品修改并經現在地市級肉制品進口藥品輔導方法局跟蹤軟件常規復查合格率后可復原制作。 附近:對昆明威寧微整形包裝材料非常有限企業著陸查驗通知