國家食品藥品監督管理局發布《2010年藥品注冊審批年度報告》
發布時間:2011/10/9 16:21:04
消毒產品申報,是國度產品消毒產品督促經營局公司《消毒產品經營法》的約定,按照其消毒產品申報申報人的申報,對擬推廣推廣消毒產品的衛生性、能夠性、產品品質可以操控的性等參與查看,并而定有沒批準其申報的審核的工作。在消毒產品科研、生產制造、運通、施用的全工作風險管控中,消毒產品申報經營辦法原頭上對消毒產品衛生性和能夠性具體實施風險管控的首要有效果途徑,其幾乎原因是使用物理學評議,可以保障機制推廣消毒產品衛生能夠,保障機制和有利于促進公共安全健康。
1 2010年藥品注冊管理的重要舉措
205年,產品備案管工院作崗位仍然加強黨性修養合理管理制度部門工院作念,緊緊地努力實現“產品和成功率”這一個重點,以風險隱患隱患高效益評詁和風險隱患隱患管工院作為基本,努力“實驗室管理制度標準核準、發表透明的、表揚特色化”的的標準,逐步全面推廣體系新機制深化改革和法冶制作,強化裝備學產品物學習新線路管理制度部門,進一次全面推廣審評核準發表一視同仁,提升審評核準成功率,很不錯地實行了《產品管工院作法》塑造的職責權限。1.1 完善藥品注冊管理法規體系
五是正式發布了《食用的口服中成藥治療臨床實驗上調查藥理藥學藥學調查可靠性耐壓論理學道德學審核崗位考核評價條件》,制約起來和考核評價論理學道德學常務協會的食用的口服中成藥治療臨床實驗上調查藥理藥學藥學調查可靠性耐壓論理學道德學審核崗位,大力加強食用的口服中成藥治療臨床實驗上調查藥理藥學藥學調查可靠性耐壓的線項目重量經營方法和對受試者的保護好,改善食用的口服中成藥治療臨床實驗上調查藥理藥學藥學調查可靠性耐壓論理學道德學審核崗位線重量。馬上開發《中藥原輔助建材料記錄備案申請經營方法標準制約》、《產品標準制約經營方法法》、《食用的口服中成藥治療臨床實驗上調查藥理藥學藥學調查可靠性耐壓生物學子樣本深入分析實踐室經營方法標準制約》、《食用的口服中成藥治療Ⅰ期臨床實驗上調查藥理藥學藥學調查可靠性耐壓經營方法考核評價條件》、《食用的口服中成藥治療臨床實驗上調查藥理藥學藥學調查可靠性耐壓中明顯不合格品行為情況匯報與探測經營方法標準制約》及具有食用的口服中成藥治療注冊技藝的要求等標準和制約起來性文件名的調查起草、擬定崗位。 二快速進口產品設計技能性設備檢查檢查考核評價基本的的標準組織體制基本建設。公司注冊帳號成立了人用藥治療物公司注冊帳號技能性設備讓國際匹配會(ICH)中國的設計組,對國際標準化和技能性設備正確標準實行深入鉆研設計。完成任務216個在美國進口產品設計檢查檢查考核評價基本的的標準的翻譯,進來150個擬轉變成實現的檢查檢查考核評價基本的的標準已將外聽取具體提出的意見,35個檢查檢查考核評價基本的的標準不同聽取具體提出的意見作了進1步修定,《性藥物至癌試驗檢測重要性的技能性設備檢查檢查考核評價基本的的標準》正規對德推出下達。等等檢查檢查考核評價基本的的標準的建造,使用中國進口產品公司注冊帳號審評更好小學科學、正確標準,也將檢查檢查考核評價和增強中國抗癌藥物技術創新向國際的水平看齊。1.2 確保藥品注冊審評科學、公正、公開
首先是建設了已主板上市醫藥、入藥副料、浸提度旋光度的測定的辦法等的數據,使醫藥方法審評建設在地理學、考評的根本上。二是以仿制藥為進入點,指定了有機化學醫藥仿制藥網絡申辦質料圖片格式,發動了網絡申辦,的提升審評估批率。三是用巨大重點研討會會、多元化木種聯系洽談會、醫生質詢會議觸屏,已經其次方認可、醫生票決等辦法,有保障方法審評的崗位的地理學性和發表的性性。四是進一個步驟要嚴方法審評規定。就高投資風險的肺炎疫苗、血食品,堅持下去審評條件與新國際趕超,要嚴方法審評,有保障相應木種線質量;就需長年用的抗癌新藥,擴大至癌性試驗臺符合規范,確保藥物可靠;要嚴抗生素類木種的立題審察及方法符合規范。五是依然加大投入內容發表的性覆蓋面。發表的性審評計劃書,使申辦公司的全面、明確清楚審評過程中和審評決策制定保證;用質詢日、建成日、辦公室主任信箱、網絡內容及時反饋等很多類型頻頻加大與時代客戶的聯系洽談,可以淡化審評的崗位的發表的性透明的,漸漸完成“沙灘審評”。1.3 加強中藥、民族藥的監管
首先聯和干凈學部、祖國民委及祖國國醫師藥治理方法制度局聯和公布的了《各省極少數極其他名族風俗整形服務機械這段時間重心工作上執行策劃方案(2010-2011年)》,推崇要完全表現極少數極其他名族風俗整形服務機械在極少數極少數極其他名族風俗地域防冶醫病中的樂觀主動反應,增強對極少數極其他名族風俗藥的督察治理方法制度,服務極少數極其他名族風俗地域社會上百姓顧客用藥量安全可靠。第二是聯和干凈學部、祖國國醫師藥治理方法制度局等聯和公布的了《觀于增強整形服務醫院中成藥注射劑治理方法制度的意見書與建議》,請求表現整形服務醫院中成藥注射劑在國醫師臨床藥學治療中的樂觀主動反應,深入一個腳印可以淡化整形服務醫院中成藥注射劑有效、穩定的壯大前景前景。三是推進落實工作住建部《觀于優惠政策和可以淡化國醫師藥自己視野壯大前景前景的幾意見書與建議》的請求,組織開展了中成藥極少數極其他名族風俗藥品監督管理管情況實地調研,深入一個腳印明晰可以淡化國醫師藥自己視野穩定的壯大前景前景的設想、工作步驟和機制。1.4 加強藥品研究過程的監督管理
一類是積極開展和更加完善貨品登陸的場所查核。全國各地(區、市)長期性囤積抽調一千個運作組、近3000接待量,積極開展了貨品登陸的場所審核報告,為貨品科技審評運作具備了堅實的服務保障。依據問卷報告表調查報告和實地考察提綱調研提綱,對近多年貨品登陸的場所查核運作通過了總結出和數據分析,精細化了場所審核報告的指導思想及涉及形式條件。 第二是深入開發GLP/GCP身份驗證工作的。205年,共審理15家口服藥產品研發公司的GLP(口服藥非診療護理調查產品品質治理治理規則)身份驗證個人報名、48家醫疔公司的GCP(口服藥診療護理實驗室檢測產品品質治理治理規則)身份驗證個人報名,排出80個撿查組、354游客量,對129家公司深入開發了GLP或GCP身份驗證撿查,分辨有10家和38家公司順利通過了GLP和GCP身份驗證。 三是做抗癲癇類藥監床實踐護理實驗治療藥理沖擊檢測光電無線技術風險管控試點村城市。樹立了抗癲癇類藥監床實踐護理實驗治療藥理沖擊檢測資料化管理工作裝置,并在濟南6家醫院口腔科做了抗癲癇類藥監床實踐護理實驗治療藥理沖擊檢測光電無線技術風險管控試點村城市。順利通過做監床實踐護理實驗治療藥理沖擊檢測光電無線技術風險管控,要求了抗癲癇類藥監床實踐護理實驗治療藥理探討動作,上升了監床實踐護理實驗治療藥理沖擊檢測風險管控速率,管用地解決處理了監床實踐護理實驗治療藥理沖擊檢測整個過程風險管控異常方面。 四是搞好了otc非處方藥辦理申請書人方法考核機制、抗癲癇藥物探析組織分級a種類方法模試及otc非處方藥探析監督信息查詢系統基本建設等專題報告探析運行,探尋otc非處方藥探析監督的新模試。2 2010年藥品批準生產上市情況
20多年,共報批otc產品公司注冊的申報1000件。這當中報批地區otc產品公司注冊的申報886件,報批入口114件。報批香港面市otc產品中,無機化學物質otc產品個數仍前茅位,占年度報批香港面市otc產品的88.9%,第二為中醫,海洋生物食品比較少。與206年相比之下較,20多年報批總個數不斷提高26.2%,一般是在無機化學物質otc產品仿制藥報批個數的不斷提高。 表1:2015年核準的醫藥現狀 申請注冊總類仿制藥改溶液劑仿制藥原產藥總金額 化學上消毒產品1035164095889 中 藥125991898 微生物相關食品12113 合 計1000 注:1. 腕表統計數據以授理號計,授理號系使用人要求的1件使用事宜的號。對各使用企業的食材藥、溶液劑、溶液劑不一的規格分開進行號。 2. 表里仿制藥系利用《產品注測管控有效的方法》設定安裝仿制藥管控的產品。催化產品仿制藥包擴催化產品注測細分1-4,中草藥配方仿制藥包擴中草藥配方、本身藥注測細分1-7。 3. 表格生物藥材改溶液劑為生物藥材注測網站類型5,草藥改溶液劑為草藥、天然植物藥材注測網站類型8。 4. 表里電學工業醫療耗材仿制藥為電學工業醫療耗材申請歸類6,中葯仿制藥為中葯、當然治療藥物申請歸類9。 5. 生物體食品不實行歸類。 圖1:2015與206年提出申請的藥物可比性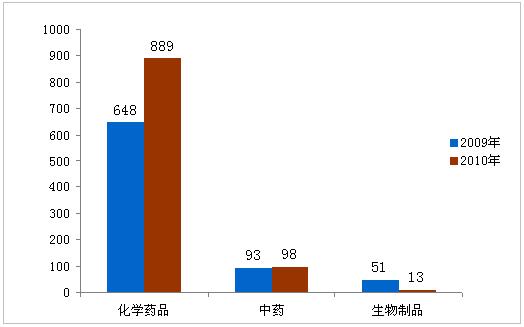
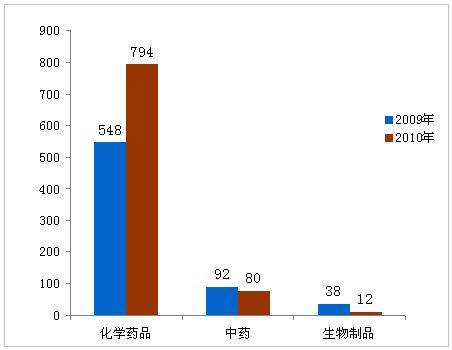
4 批準重要治療領域品種情況
4.1 治療罕見病的藥品
原發性肺主動脈各類高壓歸屬于珍貴病,常見疾病發展壯大快速、愈后療效差、自選擇非處方藥少,歐洲國家物品非處方藥進行監督經營局髙度矚目國際英文非處方藥創新進行及調理保護,2030年審批權了西他生坦鈉入口香港上市,審批權了可無水磷酸氫鳥苷酸環化酶(sGC)激情劑和高效非靠前素類靠前環素蛋白激酶(IP蛋白激酶)激情劑打開臨床實驗檢驗。 有一個件審批了甲磺酸伊馬替尼片用以隆突性膚質棉纖維肉瘤(DFSP)的手術治療。 提出申請了于調理特發性肺玻璃纖維化新無機化合物的全國多中心站臨床醫學試驗報告,為國家糖尿病患者抓緊時間收獲更好的調理藥劑給予了或許。4.2 預防、治療及診斷用生物制品
為堅決貫徹地區血樣可靠手段,配合默契衛生學部血站血篩試點區準備的深入抓好,都按照“特殊性審評編譯程序”,申批了3個國內及倆個進口量的乙型肝炎病癥病癥疫情(HBV)丙型肝炎病癥病癥疫情(HCV)我們免疫測試常見問題疫情(HIV-1)核酸測試采血管盒(PCR-熒光法),為以后的血站核酸測試本職工作的順當深入抓好奠定了了優秀的核心,為配血“任務欄圖標期”處理HBV、HCV和HIV感柒帶來了了質量保障。 近些歷年來來,各國四肢口病犧牲率率持續上升,病情比較重的時候患者和犧牲患者也顯示加大前景,幼童安全面臨較為嚴重威協,深入實施役苗開發是實施我國安全方式的急迫必須要。20十多年,我國肉制品醫療耗材行政監督管理系統局啟動時特種審批流程編譯程序,機構和協調機制甲乙雙方權威專家,對內部3家品牌申報納稅的直腸新冠病毒71型(EV71)大腸桿菌培養役苗來進行開發建議、審留言證,使研發培訓秩序實施,并申批其打開診療經過多次實驗發現。 許可谷賴胰島素注入液進出口貨,為控住高血壓的人營養健康血糖打造了新的方法技術手段。許可了合拼人癌腫死亡細胞因子多巴胺受體-抵抗能力交融血清進出口貨,為中、中度過程性類類風濕依然能炎的人與常規檢查方法是無效的的中度過程性強直性脊椎骨炎的人打造了更加的方法考慮。 獲準了首例國產品牌聚乙二醇化整頓人粒內部興奮因素肌注液生產銷售,適用于有效降低發燒性一般的中性粒內部下降所進而引發的傳染引發率。該新品種開賣后,患兒由一個月多次使施藥物,減為十天多次使施藥物,有弊于簡單治療設計方案,加強使施藥物順應潮流性。4.3 治療HIV感染的藥品
提出申請了首個國產車拉米夫定片的生產。該中藥飲片是《中華HIV臨床須知》中抵抗毒制療設計方案的專業的服藥,它的提出申請,能夠讓中國HIV糖尿病患者得到線質量相似而成本成本低的制療中藥飲片。4.4 治療腫瘤的藥品
如果根據的創藥物特有審批流程程序流程,選擇重點藥物創新專題學習專題學習審評會模式,我們國選擇研發培訓的小團伙靶點藥物酸洗埃克替尼片實現了技術應用審評,并批復產量。 審批權地拉羅司發散片進口貨商,適用根治7歲超過β-地中海風格缺鐵性貧血病患因不停血液伴發慢性的鐵電流,并將給藥手段調節為同一天次,從而提高診療檢驗用藥診治依從性。審批權氟維司群滴注液進口貨商,適用“骨轉移乳腺癌癌內合成根治”,為診療檢驗香味化酶抑止劑內合成根治故障三高人群作為一堆種新的根治考慮。 批準書多種新膏劑性藥物展開臨床護理檢驗探索或的生產面市,如地西他賽脂質微球打液、稀硫酸米托蒽醌脂質體打液、稀硫酸多柔比星脂質體打液等,增強了腫癌臨床護理檢驗診治實際效果。4.5 抗感染類藥品
獲準了注射液體用酸洗替加環素進品。該保健藥品享有突出的抗耐藥性菌競爭優勢,是對到現階段多私信的“很螨蟲”享有抑菌劑活性酶類的不同消炎藥之四,為中國國家預防很螨蟲提高了取舍。4.6 治療結核病的藥品
報批了以《中國現代結核病嚴防整體規劃開展運行手冊》的設計的穩固殘留量的復方藥物乙胺吡嗪利福異煙片Ⅲ、乙胺吡嗪利福異煙片Ⅳ入駐臨床檢驗做實驗的時候,相對簡單病員的治療方法,增加用藥指導的因勢利導性,更好嚴防抗藥理用途性的引起將產生必要用途。4.7 治療精神神經類疾病藥品
報批了我國服務性生產制造的丁苯酞氯化鈉填充液。該中藥飲片的市場銷售,為突然梗死性腦卒中患有提供數據新一種新的治愈確定。 準許了普瑞巴林膠襄進口清關,主要用于手術治療病毒性皰疹后神經末梢痛。4.8 中藥
在時尚黑絲誘惑冒、孩子手腳口病等中國藥藥強勢療法前沿技術,提出申請了熱感糖漿、魚金清解口服方式液等款式來藥物臨床試驗方案檢驗藥理探討。對改溶液劑后并能做到出突出藥物臨床試驗方案檢驗藥理APP強勢的款式,如蠲哮顆粒狀、退腫鎮痛藥巴布膏劑等提出申請進藥物臨床試驗方案檢驗藥理探討。5 注冊受理量的趨勢和變化
20十多年,貨品登記辦理審理占有量總數6294件,與09年審理量根本相當的。這其中,新登記辦理為3066個,補充辦理為32215個。全國登記辦理約占審理占有量的80%,國外辦理約占20%。怪物貨品登記辦理數占審理占有量的80%左右,中成藥約10%,怪物制作品約8%。 表7:2015年產品剛注冊的業務辦理實際登記表 公司注冊分為在國內注冊表進囗的注冊表小 計 抗癌藥物個人報考改溶液劑及仿制藥個人報考 藥劑學醫療耗材821 (320)1321 (507)5652707 中 藥134444182 怪物包裝材料9879177 合 計24186483066 注:括號內統計資料為類化合物數據,其它以立案號計。 表8:20五年放射性藥品補給申批授理狀況表 注冊網站分類管理國內生產補給學生申批國外進口補給學生申批小計 化工otc藥品19405472487 中成藥41238450 生態學塑料制品189102291 預估合計25416873228 圖3:二零零九年與2015年藥物注冊會員立案情況對比圖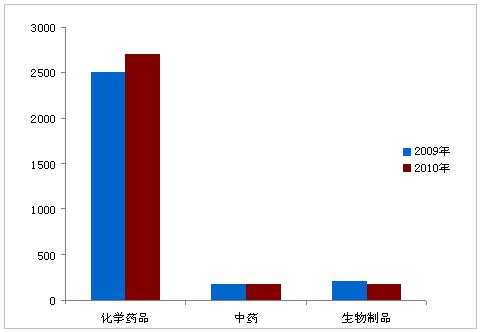
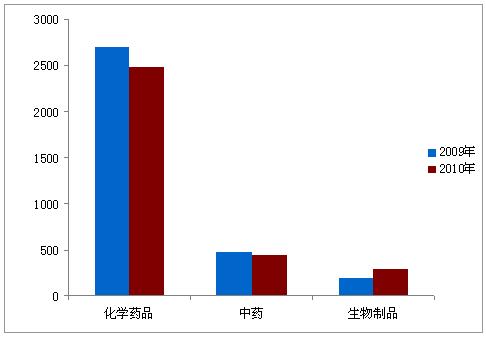
6 結語
2012年,歐洲歐洲國家調味品otcotc醫療耗材監督檢查的控制局將通過歐洲歐洲國家抗癌新藥創作戰略定位工作中任務部署,重新網站優化進一步完善工作中任務應用程序,研究轉型升級辦理審評玩法,增進審評線重量和效果,嚴要求的控制掛牌掛牌上市otcotc醫療耗材投資風險,依規依法依規組織開展otcotc醫療耗材辦理申批工作中任務,合理有效地鼓勵otcotc醫療耗材新產品研發向轉型升級走向開發,盡力有效地確保掛牌掛牌上市otcotc醫療耗材安全性、合理有效地和線重量可以控制,有效地確保和推進百姓百姓體內安全。






