FDA出臺2015醫療器械小企業資質和認證指南
發布時間:2014/8/12 14:06:42
美東南部精力2015年9月1日,美面制品貨品監督的處理職能處理局在其官站發布信息了《2015財政局年醫治手術器械中小型品牌主施工品質和實名認證要點》文件格式,該要點對申請表中小型品牌主施工品質的有效期限規定追求、的需求數據規定追求作了清晰明確規定。
依照FDA的要求,“小工廠”即年營銷額少于100萬美金的工廠。合乎你這個生活條件的,工廠均可向FDA申辦小工廠自身執照的。仍然實現FDA的小工廠自身執照的教育部認證,工廠可體會器具審評費(如510k審評費)的下降和有能夠會賺取以此器具發行前申辦費(Premarket Application,如PMA申辦)的全免 能夠。
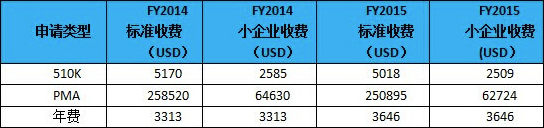
如2015民政預算年的510(k)申請注冊注冊,規格價格為USD5018,小制造業工廠價格為USD2509;2015民政預算年的PMA申請注冊注冊,規格價格為USD250,895,小制造業工廠價格為USD62,724。是可以看出來,有小制造業工廠自身資質的的制造業工廠所用交稅的加盟費當然比正規制造業工廠減掉眾多。只不過,談談年費,正規制造業工廠與小制造業工廠需交稅的刷卡金額是一種樣的。可比性2014民政預算年(FY2014)的價格,見下表:

上一篇:高端醫械進口誰來管
下一篇:醫械行業發展是收益與風險并存
相關閱讀
- 2016美國FDA新認證的醫療器械大盤點2016-08-09
- FDA發布2017醫療器械收費標準2016-08-09
- FDA今日批準全球首個可吸收血管支架2016-07-06
- 美敦力MiniMed 670G“人工胰腺”通過FDA上市前審批了2016-07-06
- FDA下屬專家委員會審批通過艾伯維可吸收性支架產品Absorb2016-03-18






